Στο MIT, μια ομάδα ερευνητών επιχειρεί να αλλάξει ριζικά τον τρόπο με τον οποίο μελετάμε τις νευροεκφυλιστικές ασθένειες. Η πιο πρόσφατη καινοτομία τους ακούει στο όνομα miBrains: τρισδιάστατοι μικροί εγκέφαλοι, στο μέγεθος ενός κέρματος, αλλά πλούσιοι σε νευρώνες, γλοιακά κύτταρα και μικροσκοπικά αιμοφόρα αγγεία. Παρά το μέγεθός τους, λειτουργούν σαν πιστή αναπαράσταση ανθρώπινου εγκεφαλικού ιστού και ήδη θεωρούνται ένα από τα πιο υποσχόμενα εργαλεία στη μάχη κατά του Alzheimer.
Το project δημιουργήθηκε υπό την καθοδήγηση της Li-Huei Tsai, μιας από τις πιο επιδραστικές μορφές στη σύγχρονη νευρολογία. Στόχος της ομάδας ήταν να ξεπεράσει τα θεμελιώδη προβλήματα των κλασικών μοντέλων: οι δισδιάστατες κυτταρικές καλλιέργειες είναι υπερβολικά απλοποιημένες, ενώ τα πειράματα σε ζώα συχνά αποτυγχάνουν να αναπαράγουν τις ιδιαιτερότητες της ανθρώπινης βιολογίας. Τα miBrains, από την άλλη, επιχειρούν να προσφέρουν μια χρυσή τομή μεταξύ ρεαλισμού και ελέγχου.
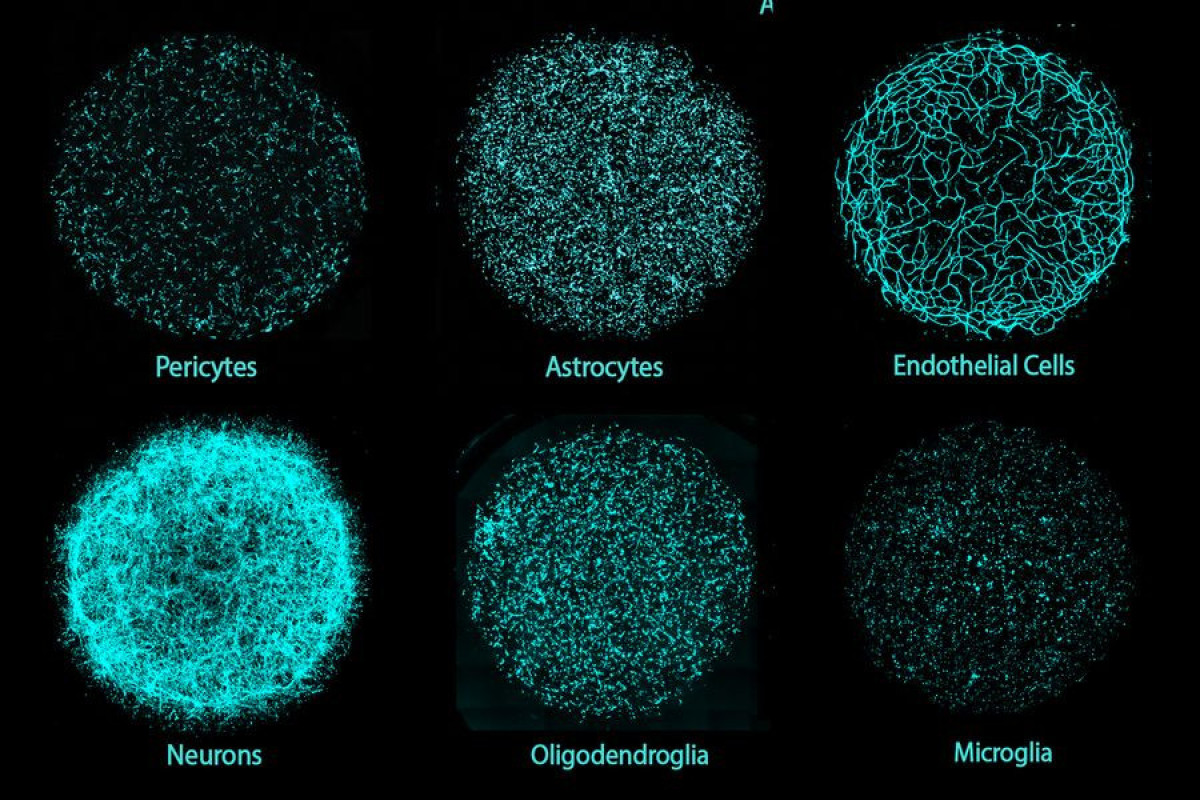
Κάθε miBrain δημιουργείται από τα βλαστοκύτταρα ενός ασθενούς, τα οποία διαφοροποιούνται σε έξι βασικούς τύπους εγκεφαλικών κυττάρων: νευρώνες, αστροκύτταρα, ολιγοδενδροκύτταρα, μικρογλοία και δύο διαφορετικά είδη αγγειακών κυττάρων. Το εντυπωσιακό είναι ότι αυτά τα κύτταρα αυτοοργανώνονται σε λειτουργικές δομές, σχηματίζοντας ακόμη και έναν ενεργό αιματοεγκεφαλικό φραγμό, το εξαιρετικά σημαντικό φίλτρο που απομονώνει το νευρικό σύστημα από την κυκλοφορία του αίματος. Η Tsai τονίζει πως αυτή τη στιγμή τα miBrains αποτελούν το μοναδικό in vitro (εργαστηριακό) μοντέλο που συγκεντρώνει όλα τα βασικά στοιχεία της ανθρώπινης εγκεφαλικής αρχιτεκτονικής.
Αυτό τα καθιστά ιδανική πλατφόρμα για πειράματα που διαφορετικά θα απαιτούσαν χρόνια ανάπτυξης ή θα ήταν αδύνατον να πραγματοποιηθούν σε ζώα. Για παράδειγμα, η ομάδα χρησιμοποίησε τα miBrains για να μελετήσει τον γονιδιακό παράγοντα κινδύνου APOE4, ο οποίος εδώ και δεκαετίες θεωρείται ο ισχυρότερος γενετικός δείκτης για την εμφάνιση Alzheimer. Στα τρισδιάστατα μοντέλα του MIT, οι ερευνητές παρατήρησαν ότι τα αστροκύτταρα που φέρουν αυτή τη γονιδιακή παραλλαγή δυσλειτουργούν στην επικοινωνία τους με τα ανοσοκύτταρα του εγκεφάλου. Το αποτέλεσμα είναι να δημιουργούνται συνθήκες που ευνοούν τη συσσώρευση των πρωτεϊνών αμυλοειδές και ταυ, οι οποίες αποτελούν κεντρικές παθολογικές υπογραφές της ασθένειας. Αυτές οι λεπτές αλληλεπιδράσεις δεν θα μπορούσαν να αποκαλυφθούν σε απλές μονοκυτταρικές καλλιέργειες.
Πίσω από την κατασκευή των miBrains βρίσκεται η neuromatrix, μια εξειδικευμένη μήτρα από υδροτζέλ που αναπτύχθηκε ειδικά για να μιμείται τη σύσταση και την ελαστικότητα του ανθρώπινου εγκεφάλου. Το σύστημα είναι πλήρως αρθρωτό: κάθε κυτταρικός τύπος μπορεί να τροποποιηθεί γενετικά, επιτρέποντας στους επιστήμονες να «προσομοιώνουν» διαφορετικές παθήσεις με ακρίβεια ή να δοκιμάζουν στοχευμένες θεραπείες πριν φτάσουν σε κλινικές δοκιμές. Για πεδία όπως η φαρμακευτική ανάπτυξη, αυτή η δυνατότητα σημαίνει ταχύτερη και πιο ασφαλή πορεία προς την ανακάλυψη νέων θεραπειών.
Ο Robert Langer, συν-συγγραφέας της μελέτης και εξέχουσα προσωπικότητα της βιοϊατρικής μηχανικής, σημειώνει ότι τεχνολογίες όπως τα miBrains θα παίξουν κρίσιμο ρόλο σε μια εποχή όπου η επιστημονική κοινότητα επιδιώκει να μειώσει δραστικά τη χρήση πειραματόζωων. Τα οφέλη είναι διπλά: όχι μόνο επιτρέπεται η άμεση δοκιμή νέων φαρμάκων σε ιστούς που μιμούνται ανθρώπινη φυσιολογία, αλλά επιτυγχάνεται και μεγαλύτερη ακρίβεια στις προβλέψεις για το πώς αυτά θα λειτουργήσουν στον πραγματικό ανθρώπινο οργανισμό.
Το MIT δεν σκοπεύει να σταματήσει εδώ. Η ομάδα ήδη εργάζεται στην ενσωμάτωση τεχνητών μικροροών αίματος και πιο προηγμένων τεχνικών γενετικής ανάλυσης, σε επίπεδο μεμονωμένων κυττάρων. Ο στόχος είναι στο σχετικά κοντινό μέλλον, κάθε ασθενής να μπορεί να έχει το δικό του προσωπικό miBrain, επιτρέποντας στους γιατρούς να προβλέπουν την εξέλιξη μιας νόσου και να δοκιμάζουν θεραπείες προσαρμοσμένες στις μοναδικές γενετικές και βιολογικές του ιδιαιτερότητες.