Σύνοψη
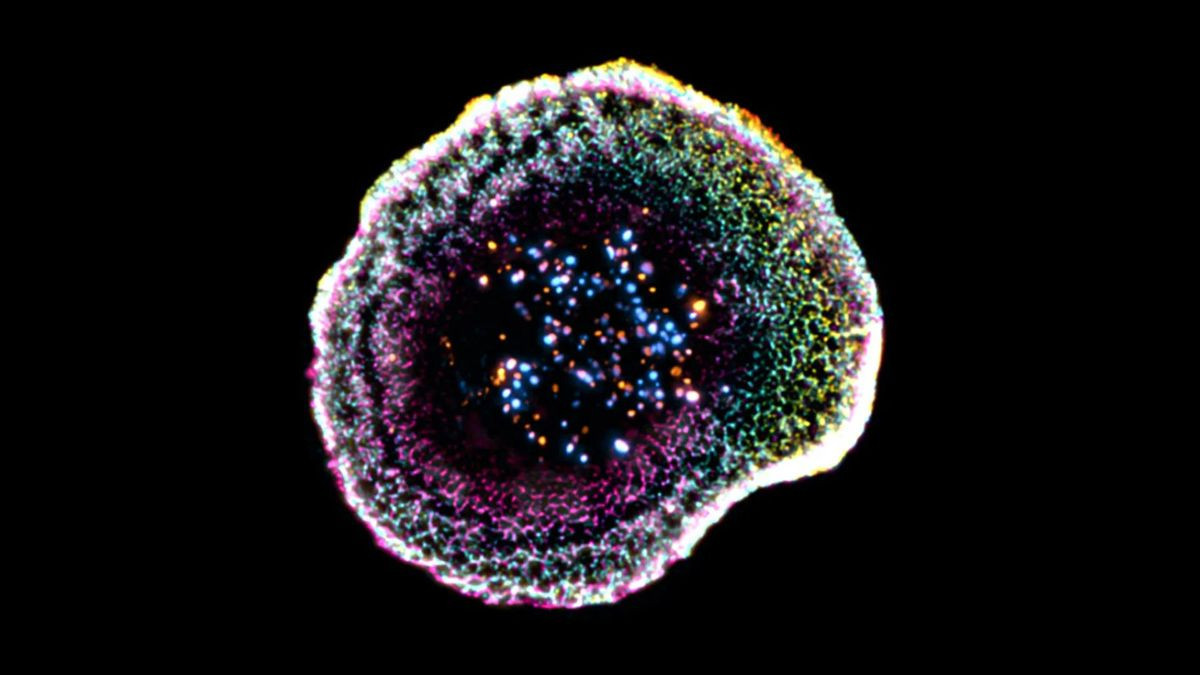
- Ερευνητές του Πανεπιστημίου της Γενεύης (UNIGE) και του Πανεπιστημιακού Νοσοκομείου της Λωζάνης (CHUV) οπτικοποίησαν για πρώτη φορά σε 3D τη διαδικασία καταστροφής καρκινικών κυττάρων από τα κυτταροτοξικά Τ-λεμφοκύτταρα.
- Χρησιμοποιήθηκε η προηγμένη τεχνική της κρυο-μικροσκοπίας διαστολής (cryo-ExM), η οποία παγώνει τα κύτταρα ακαριαία, διατηρώντας την εγγενή βιολογική τους αρχιτεκτονική.
- Αποκαλύφθηκε η δομή της «ανοσολογικής σύναψης», του ακριβούς σημείου επαφής όπου το Τ-λεμφοκύτταρο απελευθερώνει τοξικά μόρια, σχηματίζοντας έναν θόλο στη μεμβράνη.
- Η παρατήρηση επεκτάθηκε από μεμονωμένα κύτταρα σε πραγματικούς ιστούς ανθρώπινων όγκων, καταγράφοντας τη διείσδυση των Τ-λεμφοκυττάρων σε νανομετρική κλίμακα.
- Η ανακάλυψη κρίσιμα δεδομένα για την ανάπτυξη και βελτιστοποίηση θεραπειών στην ανοσο-ογκολογία.
Τα κυτταροτοξικά Τ-λεμφοκύτταρα αποτελούν την πιο εξειδικευμένη και θανατηφόρα γραμμή άμυνας του ανοσοποιητικού συστήματος. Η λειτουργία τους συνίσταται στον εντοπισμό και την ακριβή εξόντωση μολυσμένων ή καρκινικών κυττάρων στο ανθρώπινο σώμα. Η αποτελεσματικότητα τους εδράζεται σε έναν εξαιρετικά ελεγχόμενο μηχανισμό φυσικής επαφής με το κύτταρο-στόχο, ο οποίος ονομάζεται «ανοσολογική σύναψη». Μέσω αυτής της εξειδικευμένης διεπαφής, τα Τ-λεμφοκύτταρα απελευθερώνουν κυτταροτοξικά κοκκία, γεμάτα με ενεργά μόρια, εξολοθρεύοντας το καρκινικό κύτταρο χωρίς να προκαλούν την παραμικρή παράπλευρη βλάβη στους υγιείς ιστούς που το περιβάλλουν.
Η ανοσολογική σύναψη είναι η εξειδικευμένη ζώνη επαφής μεταξύ ενός Τ-λεμφοκυττάρου και ενός καρκινικού ή μολυσμένου κυττάρου. Στο σημείο αυτό, η κυτταρική μεμβράνη αναδιατάσσεται σχηματίζοντας έναν θόλο, επιτρέποντας την ασφαλή και στοχευμένη απελευθέρωση τοξικών ενζύμων, όπως η Granzyme B και η Περφορίνη, που διαλύουν το κύτταρο-στόχο εκ των έσω.
Μέχρι σήμερα, η επιστημονική κοινότητα κατανοούσε θεωρητικά τη βασική αρχή αυτού του μηχανισμού, ωστόσο η ανάλυση της λεπτομερούς δομής του σε νανομετρική κλίμακα και μάλιστα μέσα σε άθικτα ανθρώπινα κύτταρα παρέμενε αδύνατη. Οι παραδοσιακές μέθοδοι προετοιμασίας δειγμάτων αλλοίωναν συχνά τα εξαιρετικά ευαίσθητα κυτταρικά συστατικά, αναγκάζοντας τους ερευνητές να επιλέξουν μεταξύ υψηλής ανάλυσης, μεγάλου οπτικού πεδίου ή διατήρησης της φυσικής δομής του κυττάρου.
Για να ξεπεράσουν αυτούς τους περιορισμούς, οι ερευνητές εφάρμοσαν μια πρωτοποριακή μέθοδο απεικόνισης: την κρυο-μικροσκοπία διαστολής (cryo-expansion microscopy ή cryo-ExM) και η συγκεκριμένη τεχνική επιλύει το δομικό πρόβλημα των βιολογικών δειγμάτων. Η διαδικασία ξεκινά με το ακαριαίο πάγωμα των κυττάρων σε εξαιρετικά υψηλή ταχύτητα. Με αυτόν τον τρόπο, το νερό στο εσωτερικό των κυττάρων δεν προλαβαίνει να κρυσταλλοποιηθεί και μεταβαίνει σε μια «υαλώδη» κατάσταση. Αυτό το βήμα είναι κρίσιμο, καθώς οι κρύσταλλοι πάγου συνήθως καταστρέφουν την αρχιτεκτονική των κυτταρικών μεμβρανών.
Στη συνέχεια, τα δείγματα υπόκεινται σε φυσική διαστολή με τη χρήση ενός ειδικού απορροφητικού υδροτζέλ. Το υδροτζέλ «φουσκώνει» το δείγμα, μεγεθύνοντας την εσωτερική του οργάνωση χωρίς να αλλοιώνει τις σχετικές αποστάσεις και τις δομές των πρωτεϊνών. Αυτό επιτρέπει στα οπτικά μικροσκόπια να «δουν» λεπτομέρειες σε νανοκλίμακα, οι οποίες υπό κανονικές συνθήκες απαιτούν περίπλοκα και συχνά καταστροφικά ηλεκτρονικά μικροσκόπια. Η Virginie Hamel, Senior Lecturer στο Τμήμα Μοριακής και Κυτταρικής Βιολογίας της Σχολής Θετικών Επιστημών του UNIGE, τονίζει ότι η μέθοδος διατηρεί την αρχιτεκτονική των κυττάρων σε κατάσταση σχεδόν όμοια με την εγγενή (near-native).
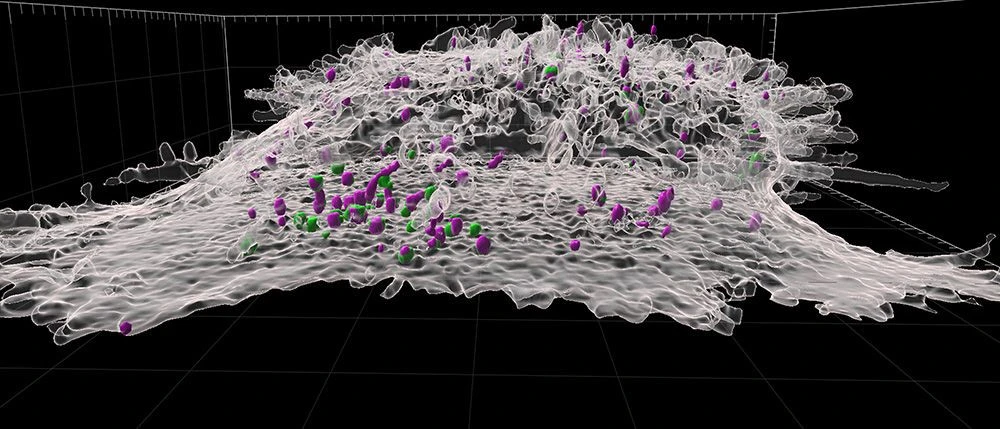
Η εφαρμογή της cryo-ExM απέδωσε άμεσα αποτελέσματα, αναδεικνύοντας προηγουμένως αθέατες δομικές λεπτομέρειες. Σύμφωνα με τον Florent Lemaître, μεταδιδακτορικό ερευνητή και κύριο συγγραφέα της μελέτης, στο σημείο επαφής μεταξύ του ανοσοποιητικού κυττάρου και του στόχου του, η μεμβράνη σχηματίζει έναν ειδικό θόλο. Αυτή η θολοειδής δομή συνδέεται άμεσα με τις αλληλεπιδράσεις προσκόλλησης και την εσωτερική οργάνωση του κυττάρου, εξασφαλίζοντας την απόλυτη σταθερότητα κατά την επίθεση.
Παράλληλα, η ομάδα κατάφερε να απεικονίσει τα κυτταροτοξικά κοκκία με πρωτοφανή διαύγεια. Αυτά τα «οπλοστάσια» των Τ-λεμφοκυττάρων βρέθηκε ότι διαθέτουν διαφορετικές εσωτερικές οργανώσεις, ενίοτε περιέχοντας έναν ή πολλαπλούς «πυρήνες» όπου συγκεντρώνονται τα ενεργά μόρια, βελτιστοποιώντας έτσι την ισχύ της επίθεσης κατά τη στιγμή της απελευθέρωσης τους.
Το σημαντικότερο βήμα της συγκεκριμένης μελέτης δεν είναι απλώς η εργαστηριακή παρατήρηση in vitro, αλλά η μετάβασή της σε κλινικό πλαίσιο. Οι ερευνητές, υπό την καθοδήγηση της Benita Wolf, Chief Resident και Associate Researcher στο Τμήμα Κλινικής Ογκολογίας του CHUV, επέκτειναν την τεχνική cryo-ExM απευθείας σε δείγματα πραγματικών ανθρώπινων όγκων.
Η παρατήρηση των Τ-λεμφοκυττάρων την ώρα που διεισδύουν στους όγκους και αναπτύσσουν τον κυτταροτοξικό τους μηχανισμό (cytotoxic machinery) μέσα στον καρκινικό ιστό, προσφέρει μια ρεαλιστική αποτύπωση των φυσιολογικών περιορισμών. Η κατανόηση του πώς τα ανοσοκύτταρα αντιμετωπίζουν το φυσικό περιβάλλον του όγκου μπορεί να εξηγήσει γιατί ορισμένες ανοσοθεραπείες αποτυγχάνουν και ποιες τροποποιήσεις απαιτούνται για να ενισχυθεί η διεισδυτικότητά τους.
Η μελέτη θέτει ένα νέο δομικό πλαίσιο αναφοράς. Η δυναμική αυτή μπορεί να επηρεάσει άμεσα τη φαρμακολογία και το σχεδιασμό νέων ανοσοθεραπειών, προσφέροντας δεδομένα για την τροποποίηση των CAR-T λεμφοκυττάρων ώστε να σχηματίζουν πιο αποδοτικές ανοσολογικές συνάψεις.
*Μπορείτε πλέον να προσθέσετε το Techgear.gr ως Προτιμώμενη Πηγή ενημέρωσης για τις αναζητήσεις σας στο Google Search!