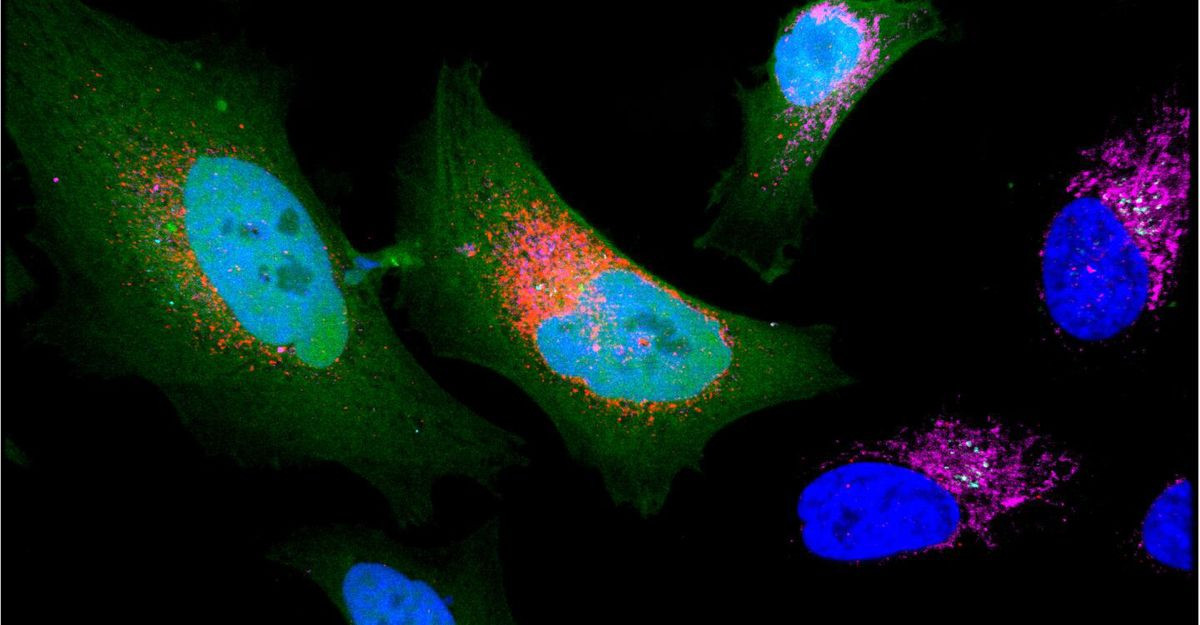
Μια σημαντική ανακάλυψη από ερευνητές του Weill Cornell Medicine ρίχνει φως σε έναν από τους πιο επιθετικούς τύπους καρκίνου του μαστού και ανοίγει τον δρόμο για νέες θεραπείες. Οι επιστήμονες εντόπισαν ότι ένα ένζυμο, γνωστό ως EZH2, λειτουργεί σαν «καταλύτης του χάους» μέσα στα κύτταρα του τριπλά αρνητικού καρκίνου του μαστού (TNBC), οδηγώντας σε ανεξέλεγκτες κυτταρικές διαιρέσεις και στη διασπορά του καρκίνου σε άλλα όργανα. Όταν το ένζυμο αυτό μπλοκαρίστηκε, η κυτταρική σταθερότητα αποκαταστάθηκε και η εξάπλωση των καρκινικών κυττάρων σταμάτησε.
Ο επικεφαλής της έρευνας, Dr. Vivek Mittal, καθηγητής στο Weill Cornell Medicine και μέλος του Sandra and Edward Meyer Cancer Center, εξηγεί ότι η μετάσταση είναι η κύρια αιτία θνησιμότητας στους ασθενείς με TNBC. «Η μελέτη μας δείχνει έναν νέο τρόπο να σταματήσουμε τη μετάσταση πριν καν ξεκινήσει», σημειώνει. Τα αποτελέσματα δημοσιεύθηκαν στο περιοδικό Cancer Discovery στις 2 Οκτωβρίου και ανατρέπουν την επικρατούσα θεωρία ότι οι θεραπείες κατά του καρκίνου θα πρέπει να επιτείνουν τα σφάλματα διαίρεσης στα καρκινικά κύτταρα μέχρι αυτά να καταρρεύσουν.
Σε φυσιολογικές συνθήκες, όταν ένα κύτταρο διαιρείται, τα χρωμοσώματα αντιγράφονται και μοιράζονται ομοιόμορφα στα δύο θυγατρικά κύτταρα. Στον καρκίνο, όμως, αυτός ο μηχανισμός συχνά διαταράσσεται, προκαλώντας χρωμοσωμική αστάθεια: μερικά κύτταρα λαμβάνουν υπερβολικά ή ελλιπή χρωμοσώματα, οδηγώντας σε μια «γενετική αναρχία» που ευνοεί την εξέλιξη του όγκου. Ο Dr. Mittal προειδοποιεί ότι η σκόπιμη ενίσχυση αυτής της αστάθειας, όπως προτείνουν ορισμένες θεραπείες, μπορεί να έχει το αντίθετο αποτέλεσμα: «Αν δεν επιτευχθεί το σωστό επίπεδο, η τακτική αυτή μπορεί να κάνει τον καρκίνο πιο επιθετικό». Η δική του ομάδα, αντίθετα, αναζητά τρόπους να επαναφέρει την τάξη στη διαίρεση των κυττάρων, στοχεύοντας απευθείας το ένζυμο EZH2.
Η πρώτη συγγραφέας της μελέτης, Dr. Shelley Yang Bai, ξεκίνησε την έρευνα ως μεταπτυχιακή φοιτήτρια και τη συνέχισε ως μεταδιδακτορική συνεργάτιδα του Dr. Mittal, ενώ στη μελέτη συμμετείχε και ο Dr. Samuel Bakhoum από το Memorial Sloan Kettering Cancer Center. Η ομάδα τους επιχείρησε να κατανοήσει πώς η επιγενετική –οι χημικές μεταβολές που επηρεάζουν τη λειτουργία των γονιδίων χωρίς να αλλάζουν το DNA– συνδέεται με τη μετάσταση.
Μόνο ένα μικρό ποσοστό, περίπου 5%, των κυττάρων ενός πρωτογενούς όγκου TNBC έχει τη δυνατότητα να εξαπλωθεί σε απομακρυσμένα όργανα. Αυτά τα κύτταρα ξεχωρίζουν για το διαφορετικό τους μεταβολισμό, τη μεγάλη χρωμοσωμική αστάθεια και τις επιγενετικές αλλοιώσεις τους. Η έρευνα έδειξε ότι ο βασικός υπαίτιος αυτών των χαρακτηριστικών είναι το ένζυμο EZH2, το οποίο σε φυσιολογικά κύτταρα ρυθμίζει τη δομή του DNA. Στα καρκινικά κύτταρα όμως, η υπερπαραγωγή του EZH2 «σιωπά» κρίσιμα γονίδια που είναι υπεύθυνα για την ορθή κατανομή των χρωμοσωμάτων κατά τη διαίρεση, προκαλώντας εκτεταμένα λάθη.
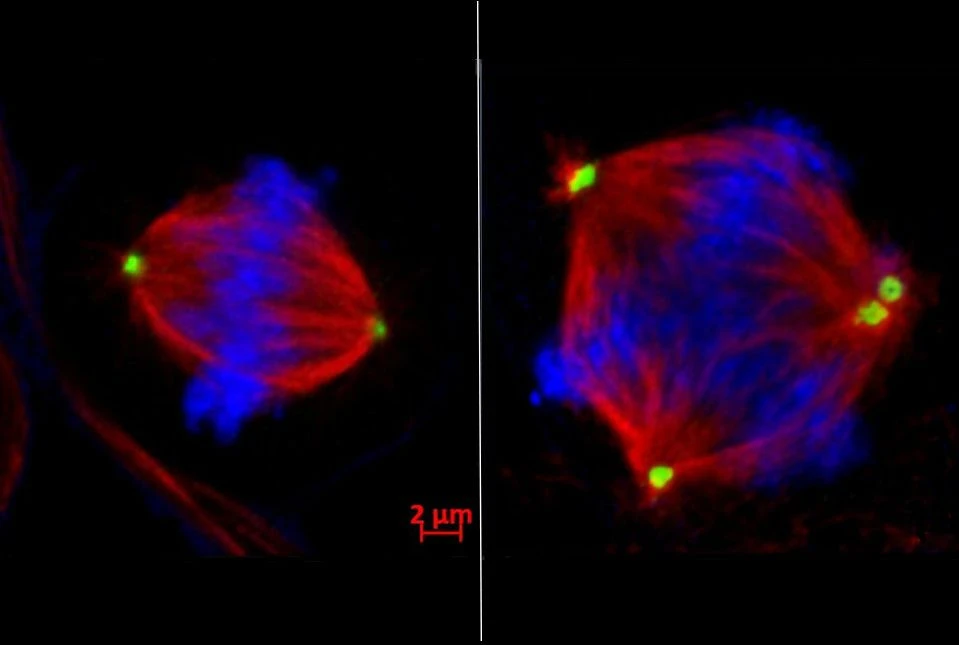
Αναλύοντας δεδομένα από ασθενείς με καρκίνο του μαστού, η Dr. Bai παρατήρησε ότι όσοι είχαν υψηλότερα επίπεδα EZH2 παρουσίαζαν και περισσότερες χρωμοσωμικές ανωμαλίες στους όγκους τους. Αυτό αποτέλεσε την αφετηρία για μια σειρά πειραμάτων στο εργαστήριο. Οι ερευνητές χρησιμοποίησαν το φάρμακο ταζεμετοστάτη –το οποίο ήδη έχει εγκριθεί από τον FDA για άλλες μορφές καρκίνου– και διαπίστωσαν ότι αναστέλλοντας το EZH2 μειώνονταν οι διαταραχές στη διαίρεση των κυττάρων. Αντίθετα, η τεχνητή αύξηση του EZH2 οδήγησε σε ακόμα μεγαλύτερη αστάθεια.
Σε πειράματα με ποντίκια, οι όγκοι που παρήγαγαν υψηλά επίπεδα του ενζύμου εμφάνισαν πολύ περισσότερες μεταστάσεις στους πνεύμονες, επιβεβαιώνοντας τη σύνδεση ανάμεσα στο EZH2, την αστάθεια των χρωμοσωμάτων και την εξάπλωση του καρκίνου.
Η ομάδα αποκάλυψε και τον ακριβή μηχανισμό: το EZH2 καταστέλλει το γονίδιο τανκυράση 1, το οποίο κανονικά εξασφαλίζει τη σωστή λειτουργία του συστήματος που χωρίζει τα χρωμοσώματα. Όταν αυτό το γονίδιο «σιωπά», μια άλλη πρωτεΐνη, η CPAP, συσσωρεύεται υπερβολικά, προκαλώντας ανεξέλεγκτο πολλαπλασιασμό των κεντροσωμάτων — των δομών που τραβούν τα χρωμοσώματα στις δύο πλευρές του κυττάρου. Το αποτέλεσμα είναι χαοτικές διαιρέσεις και δημιουργία πολλαπλών θυγατρικών κυττάρων με αλλοιωμένο γενετικό υλικό.
Όταν όμως οι ερευνητές ανέστειλαν το EZH2, η ισορροπία αποκαταστάθηκε. Οι μεταστάσεις μειώθηκαν δραματικά και η σταθερότητα των χρωμοσωμάτων επανήλθε. «Για πρώτη φορά συνδέουμε ένα επιγενετικό ρυθμιστή, όπως το EZH2, με τη χρωμοσωμική αστάθεια με μηχανιστικό τρόπο», τόνισε η Dr. Bai.
Η Dr. Magdalena Plasilova, χειρουργός ογκολόγος στο NewYork-Presbyterian/Weill Cornell Medical Center, υπογραμμίζει τη σημασία της ανακάλυψης:
Η μελέτη αυτή ανοίγει έναν νέο δρόμο για τη θεραπεία του τριπλά αρνητικού καρκίνου του μαστού, στοχεύοντας την ίδια τη ρίζα της μετάστασης. Βλέπω καθημερινά τις επιπτώσεις που έχει η διασπορά του καρκίνου στους ασθενείς – αυτή η ανακάλυψη φέρνει πραγματική ελπίδα.
Ο Dr. Mittal επισημαίνει ότι η ταζεμετοστάτη θα μπορούσε να επαναξιοποιηθεί για τη θεραπεία του TNBC, ενώ ίσως και άλλες ενώσεις να αποδειχθούν ακόμη πιο αποτελεσματικές. Ήδη σχεδιάζονται κλινικές δοκιμές για να αξιολογηθεί η ασφάλεια και η αποτελεσματικότητα αυτών των φαρμάκων όχι μόνο στον καρκίνο του μαστού, αλλά και σε άλλους τύπους που χαρακτηρίζονται από παρόμοια χρωμοσωμική αστάθεια, όπως ο καρκίνος του πνεύμονα.
«Αν μπορέσουμε να ελέγξουμε τη χρωμοσωμική αστάθεια, θα μπορέσουμε να ελέγξουμε και τη μετάσταση», καταλήγει ο Dr. Mittal. «Και αυτό θα μπορούσε να αλλάξει ριζικά την πορεία μιας από τις πιο θανατηφόρες μορφές καρκίνου».
[via]